| |
Keul-o-test
TSH Test
für Vollblut, Serum und Plasma
Bestellnummer: KGST 136
DIMDI-Reg.-Nr.: DE/CA22/1116-171-IVD
VERWENDUNGSZWECK
Der Keul-o-test TSH (thyroid stimulating hormone, schilddrüsenstimulierendes Hormon) ist zur qualitativen Bestimmung von TSH, auch bekannt als Thyrotropin oder auch als thyrotrophes Hormon, vorgesehen. Es kann Vollblut, Serum oder Plasma verwendet werden. Der Nachweis von TSH, welches vom Hypophysenvorderlappen ausgeschüttet wird, dient als Hilfe bei der Diagnose der Unterfunktion der Schilddrüsen- oder Hypophysen-Fehlfunktion. Der TSH Test ist ein immunochromatographischer Assay. Die Nachweisgrenze liegt bei 5 µIU/ml.
LIEFERUMFANG
- TSH-Testkassette mit Pipette im Folienbeutel (25 pro Kitbox)
- Gebrauchsanweisung (1 pro Kitbox)
BENÖTIGT, JEDOCH NICHT MITGELIEFERT
-
Stoppuhr
-
Lanzette (bei Blutentnahme aus der Fingerkuppe)
-
heparinisierte Kapillare (bei Blutentnahme aus der Fingerkuppe)
Zur Beachtung
Der Keul-o-test TSH soll bei 2-30oC gelagert werden. Die Testkassette ist gegenüber Feuchtigkeit und Hitze empfindlich. Verwenden Sie den Test unverzüglich, nachdem Sie ihn dem Folienbeutel entnommen haben. Nicht nach Ablauf des Verfalldatums anwenden.
Der TSH Test kann mit Vollblut (venös oder aus Fingereinstich versetzt mit Na- oder Li-Heparin als Antikoagulanz), Serum oder Plasma durchgeführt werden.
TESTDURCHFÜHRUNG
| 1 |
Entnehmen Sie die Testkassette aus dem Folienbeutel und legen Sie sie auf eine flache, trockene und saubere Oberfläche. |
| 2 |
Serum oder Plasma |
Venöses Vollblut |
Vollblut aus Fingereinstich |
| 3 |
Träufeln Sie nacheinander (warten Sie stets bis der jeweilige Tropfen absorbiert wurde, bevor Sie den nächsten Tropfen zufügen. Es kann besonders bei Blut, durch zu schnelles Träufeln zu Verklumpungen führen) mit der beiliegenden Pipette 3 hängende Tropfen Serum oder Plasma (etwa 120µl) in das Probenfeld (S) des TSH Tests.
Falls nach 30 Sekunden keine violette Fließbewegung im Ergebnisfenster zu sehen ist, fügen Sie einen vierten Tropfen hinzu. |
Träufeln Sie nacheinander (warten Sie stets bis der jeweilige Tropfen absorbiert wurde, bevor Sie den nächsten Tropfen zufügen. Es kann besonders bei Blut, durch zu schnelles Träufeln zu Verklumpungen führen) mit der beiliegenden Pipette 3 hängende Tropfen heparinisiertes Vollblut (etwa 120µl) in das Probenfeld (S) des TSH Tests. Die benötigte Tropfenanzahl kann je nach Volumen pro Tropfen variieren!
Falls nach 30 Sekunden keine violette Fließbewegung im Ergebnisfenster zu sehen ist, fügen Sie einen vierten Tropfen hinzu. |
Träufeln Sie nacheinander (warten Sie stets bis der jeweilige Tropfen absorbiert wurde bevor Sie den nächsten Tropfen zufügen. Es kann besonders bei Blut, durch zu schnelles Träufeln zu Verklumpungen führen) 3 mit einer heparinisierten Kapillare aus der Fingerkuppe gewonnene, hängende Tropfen Vollblut
(etwa 120µl) in das Probenfeld (S) des TSH Tests. Die benötigte Tropfenanzahl kann je nach Volumen pro Tropfen variieren!
Falls nach 30 Sekunden keine violette Fließbewegung im Ergebnisfenster zu sehen ist, fügen Sie einen vierten Tropfen hinzu. |
| |
|
|
|
| 4 |
Beginnen Sie die Zeit zu stoppen. Warten Sie darauf, dass die rote(n) Linie(n) erscheint bzw. erscheinen. Lesen Sie das Ergebnis nach 10 Minuten ab. Lesen Sie nach mehr als 15 Minuten keine Ergebnisse mehr ab. |
Vorsicht: Die angegebene Auswertezeit gilt für eine Umgebungstemperatur von 15 bis 30oC. Falls der Test bei niedrigerer Temperatur durchgeführt wird, muß die Zeit entsprechend verlängert werden.
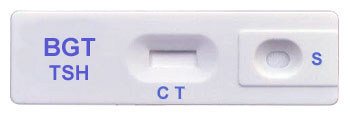
AUSWERTUNG
- Eine farbige Kontroll-Linie erscheint im mit „C“ markierten Teil des Ergebnisfensters. Sie bestätigt die korrekte Funktion des Tests.
- Im mit „T“ markierten Teil des Ergebnisfensters wird das Testresultat angezeigt. Die dort erscheinende Linie ist die Testlinie
Von Links nach Rechts:
Positiv – Negative – Ungültig – Ungültig
Positiv: Zwei Linien („T“ and „C“) erscheinen im Ergebnisfenster. Dabei spielt keine Rolle, welche Linie zuerst sichtbar wird (Abb. 1). Bemerkung: Die Testlinie wird um so dunkler ausfallen, je höher die TSH-Konzentration ist. Liegt die TSH-Konzentration nahe an der Nachweisgrenze, wird die T-Linie nur sehr schwach ausgeprägt sein.
Negativ: Nur die C-Linie ist vorhanden (Abb. 2).
Ungültig: Falls nach Testdurchführung nur eine Linie bei „T“ oder gar keine Linie erscheint, ist der Test ungültig (Abb. 3 und 4). Möglicherweise wurde der Test nicht richtig ausgeführt oder das Verfalldatum ist überschritten. In diesem Fall muß ein neuer Test durchgeführt werden.
Bemerkung: Ein positives Resultat wird auch nach mehr als 15 Minuten korrekt angezeigt. Wird der Test jedoch nach mehr als 15 Minuten ausgewertet, ist es möglich, dass auch kleinere TSH-Konzentrationen als 5 mIU/ml ein positives Ergebnis zeigen. Proben mit einer hohen Konzentration an Rheumafaktoren können ein unspezifisches positives Resultat hervorrufen
SENSITIVITÄT UND SPEZIFITÄT
Die Empfindlichkeit des TSH-Test beträgt 5 µlU/ml TSH. Die Fähigkeit des Testes speziell TSH zu erkennen wurde durch Kreuz-Reaktions-Studien untersucht, bei der Proben, die bekannten Mengen von strukturell und physiologisch verwandten Hormonen enthielten, verwendet wurden. Vollblut- und Serumproben mit 500 mlU/ml LH (humanes luteinisierendes Hormon), 1000 mlU/ml FSH (follikelstimulierendes Hormon), 200,000 mlu/ml hCG (humanes Choriongonadotropin) zeigen negative Ergebnisse.
EINSCHRÄNKUNGEN
Obwohl der Keul-o-test TSH TSH sehr präzise bestimmt, können falsche Resultate nicht ganz ausgeschlossen werden. Es müssen weitere Untersuchungen ausgeführt werden, falls der TSH-Test ein zweifelhaftes Resultat liefert.
Wie bei allen klinischen Tests darf eine Diagnose nicht nur auf einem Testergebnis beruhen, sondern alle klinischen Befunde und Untersuchungsergebnisse müssen vom Arzt zur Beurteilung herangezogen werden
WARNHINWEISE
- Die Lanzette darf nur einmal für eine Person verwendet werden, da sonst die Gefahr der Übertragung gefährlicher Krankheiten besteht.
- Dekontaminieren Sie alle mit Probenmaterial in Berührung gekommenen Gegenstände und entsorgen Sie sie gemäß den geltenden Bestimmungen.
- Nicht nach Ablauf des Verfalldatums verwenden.
- Test nicht verwenden, wenn der Folienbeutel eingerissen oder beschädigt ist.
- Nur für die In-vitro-Diagnostik.
LITERATUR
- Brennan MD, Klee GG, Preissner CM, et al, „Heterophilic Serum Antiodies: A Cause for Falsely Elevated Serum Thyrotropin Levels,“ Mayo Clin Proc, 1987, 62:894-98.
- Cooper DS, „Thyroid Hormone Treatment: New Insights Into an Old Therapy,“ JAMA, 1989, 261(18):2694-5.
- Gorman CA, „Symposium on Sensitivity TSH Assays – Introduction: Thyroid Function Testing: A New Era,“ Mayo Clin Proc, 1988, 63:1026-7.
- Hamblin PS, Dyer SA, Mohr VS, et al, „Relationship Between Thyrotropin and Thyroxine Changes During Recovery From Severe Hypothyroxinemia of Critical Illness,“ J Clin Endocrinol Metab, 1986, 62:717-22.
- Klee GG, „Symposium on Sensitive TSH Assays – Part II: Sensitive Thyrotropin Assays: Analytic and Clinical Performance Criteria,“ Mayo Clin Proc, 1988, 63:1123-32.
- Martinez M, Derksen D, and Kapsner P, „Making Sense of Hypothyroidism. An Approach to Testing and Treatment,“ Postgrad Med, 1993, 93(6): 135-8, 141-5.
- Rosenfeld L and Blum M, „Immunoradiometric Assay for Thyrotropin (TSH) Should Replace the RIA Method in the Clinical Laboratory,“ Clin Chem, 1986, 32:232-3,(letter).
- Sawin CT, Geller A, Hershman JM, et al, „The Aging Thyroid: The Use of Thyroid Hormone in Older Persons,“ JAMA, 1989, 261(18):2653-5.
- Surks MI, „Guidelines for Thyroid Testing,“ Lab Med, 1993, 24(5):270-4.
Qualitätssicherung und Vorkommnisse
Sollten Sie den Eindruck eines Qualitätsmangels haben oder unklare oder ihrerseits falsch-positive oder falsch-negative Ergebnisse erhalten, bitten wir Sie, die betreffende Patientenprobe zurückzustellen und für einen Abruf für uns bereitzuhalten.
Bitte informieren Sie uns umgehend. Sie helfen uns dadurch die Sicherheit der Produkte und damit die Qualität zu gewährleisten.
Abrechnung
| |
Nr. |
Preis in € |
| GOÄ |
4030 |
16,76 |
 |
Hersteller: |

Günter Keul GmbH
Von-Langen-Weg 10
D-48565 Steinfurt
Tel.: 02551/2097 Fax.: 02551/80883
Web: www.keul.de |
(akt. 30.04.2015)
|
|