| |
-o-test®
D-Dimer
Testkassette für Vollblut und Plasma
KGST172
DIMDI-Reg.-Nr.: DE/CA22/1116-184-IVD
Ein Schnelltest für die Diagnose des Herzinfarkts (MI) zum qualitativen Nachweis von D-dimer im Vollblut oder Plasma.
Nur für die professionelle In-vitro-diagnostische Verwendung.
VERWENDUNGSZWECK
Der D-Dimer Kassettentest ist ein visueller Schnelltest zum qualitativen Nachweis von D-Dimer in Plasma oder Vollblut. Dieser Test soll als Hilfe bei der Diagnose disseminierter intravasaler Gerinnungsstörungen (DIC), tiefer Venenthrombose (TVT) und Lungenembolie dienen und ist nur für den in-vitro-diagnostischen Gebrauch durch professionelle Anwender gedacht.
ZUSAMMENFASSUNG
Tests auf D-Dimer wurden ursprünglich in der Diagnose disseminierter intravasaler Gerinnungsstörungen (DIC) entwickelt. In den 90er Jahren erkannte man ihren Nutzen in der Diagnose thromboembolischer Prozesse. D-Dimer ist ein Fibrin-Abbauprodukt, ein kleines Eiweißfragment, das nach dem Abbau eines Blutgerinnsels mittels Fribronolyse im Blut vorhanden ist. Während der Blutgerinnung wird das Fibrinogen durch die Aktivierung von Thrombin zu Fibrin verstoffwechselt. Fibrin besteht aus D- und E-Einheiten. Die Spaltung von Fibrin führt zu so genannten D-Dimeren. Zur Unterstützung einer Thrombosediagnostik kann die D-Dimerkonzentration mit Hilfe eines Bluttests bestimmt werden. Seit seiner Einführung in den 90er Jahren hat sich diese Bestimmung zu einem wichtigen Test bei Patienten mit Verdacht auf Thrombose-Erkrankungen entwickelt. Während ein negatives Ergebnis Thrombose praktisch ausschließt, kann ein positives Ergebnis eine Thrombose indizieren, schließt aber andere mögliche Krankheiten nicht aus. Sein Hauptnutzen besteht also im Ausschluss thromboembolischer Krankheiten, wenn deren Wahrscheinlichkeit gering ist. D-Dimer-Tests sind von klinischem Nutzen, wenn Verdacht auf tiefe Venenthrombose (TVT) oder Lungenembolie (PE) besteht. Bei Patienten mit Verdacht auf disseminierte intravasale Gerinnungsstörung (DIC) kann ein Test auf D-Dimer die Diagnose unterstützen.
ARBEITSWEISE
Der D-Dimer Kassettentest ist für den Nachweis von D-Dimer in Plasma oder Vollblut vorgesehen. Diese Information kann von Arzt und Patient für die Behandlung genutzt werden. Der D-Dimer Kassettentest wurde auf den Nachweis von D-Dimer in Plasma oder Vollblut mittels visueller Interpretation der Farbentwicklung in der Testkassette, einem Sandwich-Immunoassay, ausgelegt. Die Membran wurde in der Testlinienregion (T) mit einem Antikörper gegen D-Dimer beschichtet. Während des Tests kann die verdünnte Probe mit einem gefärbten Konjugat (anti-D-Dimer Antikörper-Goldkonjugat) reagieren, das auf den Pad im Inneren der Testkassette gegeben wurde. Das Gemisch bewegt sich dann chromatographisch mittels Kapillarwirkung über die Membran. Ist in der Probe D-Dimer vorhanden, wird in der Testlinienregion (T) der Membran eine farbige Linie mit einem spezifischen Antikörper-Antigen-Konjugatkomplex ausgebildet. Dieser Komplex besteht aus einem gefärbten anti-D-Dimer-Antikörper, D-Dimer aus der Probe unddem auf der Membran in der Testlinienregion (T) fiierten Antikörper. Andererseits er-scheint in der Kontrollregion (C) immer eine farbige Linie. Hierzu wird eine andereAntigen-Antikörperreaktion (mit Antimaus-Antikörpern) genutzt. Diese Kontrolllinie dientals Verfahrensindikator für die ordnungsgemäße Funktion des Kits. Sie zeigt an, dass das Testverfahren korrekt abgelaufen und die Probe ordnungsgemäß über die Membran geflssen ist. Eine ausgeprägte Farbentwicklung in der Testlinienregion (T) zeigt einpositives Ergebnis an. Das Fehlen einer Farblinie in der Testlinienregion (T) weist auf ein negatives Ergebnis hin.
REAGENZIEN
Der Test enthält mit anti- D-Dimer Antikörper beschichtete kolloidale Goldpartikel und eine mit einem Fangreagenz beschichteten Membran.
VORSICHTSMASSNAHMEN
- Nur für den in-vitro-diagnostischen Gebrauch durch professionelle Anwender!
- Kit nicht nach Ablauf des Haltbarkeitsdatums verwenden.
- Vor Durchführung des Test die Anleitung genau lesen.
- Nicht benutzen, wenn der Folienbeutel Beschädigungen aufweist, weil der Test empfindilch gegen Feuchtigkeit ist.
- Folienbeutel erst öffnen, wenn Sie zur Durchführung des Tests bereit sind.
- Nicht zweimal verwenden!
- In den Bereichen, in denen mit Probenmaterial oder Tests gearbeitet wird, sind Essen, Trinken oder Rauchen untersagt.
- Alles Probenmaterial von Patienten ist als potentiell infektiös zu behandeln. Beachten Sie bitte während des gesamten Tests alle bewährten Vorsichtsmaßnahmen zum Umgang mit biologisch gefährlichen Materialien, und befolgen Sie die Standardverfahren zur ordnungsgemäßen Entsorgung von Probenmaterial.• Die Verdünnungslösung enthält geringere Mengen von ProClin300 (0,02%) als Konservierungsmittel.
- Reagenzien nicht mit dem Mund pipettieren!•Keine Lösung in das Reaktionsfenster spritzen!
- Das Reaktionsfenster des Kits nicht berühren, damit Verunreinigungen vermieden werden!
- Beim Testen von Probenmaterial Schutzkleidung wie Laborkittel, Einweghandschuhe und Augenschutz tragen.
- Die Testkassette immer bei 2 – 30°C (36° – 86°F) lagern und transportieren.
- Feuchtigkeit und hohe Temperaturen können die Ergebnisse beeinträchtigen.
LAGERUNG UND STABILITÄT
Das Testkit kann über die gesamte Haltbarkeitsdauer gekühlt (2-8°C) oder bei Raumtemperatur (bis 30°C) gelagert werden.
PROBENAHME UND VORBEREITUNG
- Die D-Dimer-Schnelltestkassette (Vollblut/ Plasma) kann mit Vollblut (durch Venenpunktion oder Fingereinstich) oder Plasma durchgeführt werden.
- Zur Probenahme vom Vollblutproben aus Fingereinstich:
- Waschen Sie die Hand des Patienten mit Seife und warmen Wasser oder reinigen Sie sie mit einem Alkoholtupfer. Warten Sie bis sie trocken ist.
- Massieren Sie die Hand ohne die Punktionsstelle zu berühren mittels Abwärtsreiben der Hand zu den Fingerspitzen des Mittel- oder Ringfingers.
- Punktieren Sie die Haut mit einer sterilen Lanzette. Wischen Sie das erste Anzeichen von Blut weg.
- Reiben Sie behutsam die Hand vom Handgelenk bis zum Finger, um einen runden Tropfen an der Einstichstelle auszubilden.
- Geben Sie das Fingereinstich-Vollblut mittels eines Kapillarröhrchens in den Test:
- Tauchen Sie das Ende des Kapillarröhrchens in das Blut, bis es etwa zu 75 µL gefüllt ist. Vermeiden Sie Luftblasen.
- Setzen Sie einen Ball auf das obere Ende des Kapillarröhrchens, drücken Sie dann den Ball um das Vollblut in den Probenbereich der Testkassette zu geben.
- Hinzufügen von Fingereinstich-Vollblut zum Test mittels hängender Tropfen:
- Halten Sie den Finger des Patienten so, dass der Blutstropfen über dem Probenbereich der Testkassette ist.
- Erlauben Sie, dass 3 hängende Tropfen des Fingereinstich-Vollbluts in das Zentrum des Probenbereiches der Kassette fallen, oder bewegen Sie den Finger des Patienten so, dass die hängenden Tropfen das Zentrum des Probenbereiches berühren. Vermeiden Sie eine direkte Berührung des Fingers mit dem Probenbereich.
- Trennen Sie so bald wie möglich Serum oder Plasma vom Blut um Hämolyse zu vermeiden. Verwenden Sie nur klare, nicht hämolysierte Proben.
- Die Testdurchführung sollte unmittelbar nach der Probenahme erfolgen. Lassen Sie die Proben nicht für längere Zeit bei Raumtemperatur stehen. Serum- und Plasmaproben können bei 2-8°C für bis zu 2 Tage gelagert werden Für eine längere Lagerung sollten die Proben bei unter -20°C aufbewahrt werden. Durch Venenpunktion gewonnenes Vollblut sollte bei 2-8°C gelagert werden, wenn der Test innerhalb von einem halben Tag nach der Probenahme durchgeführt wird. Vollblutproben nicht einfrieren. Durch Fingereinstich gewonnenes Vollblut sollte unverzüglich getestet werden.
- Bringen Sie vor dem Testen die Proben auf Raumtemperatur. Eingefrorene Proben müssen vor dem Testen vollständig aufgetaut und gut durchmischt werden. Proben sollten nicht wiederholt eingefroren und aufgetaut werden.
- Wenn die Proben versandt werden, sollten Sie entsprechend den örtlichen Vorschriften betreffend des Transports von Erregern verpackt werden.
MATERIALIEN
Vorhandene Materialien
- Testkassetten
- Pipetten
- Puffer
- Gebrauchsanweisung
Erforderliche aber nicht vorhandene Materialien
- Probenahmebehälter
- Zentrifuge
- Timer
Für Fingereinstich-Vollblut
- Lanzetten
- Heparinisierte Kapillarröhrchen und Saugbällchen
GEBRAUCHSANWEISUNG
Erlauben Sie dem Test, der Probe, dem Puffer und/oder den Kontrollen vor dem Test Raumtemperatur (15-30°C) zu erreichen.
- Bringen Sie die Folientasche auf Raumtemperatur, bevor Sie sie öffnen. Entnehmen Sie die Testkassette aus dem versiegelten Folienbeutel und verwenden Sie sie innerhalb einer Stunde.
- Legen Sie die Testkassette auf eine saubere und ebene Oberfläche.
Für Plasmaproben:
• Halten Sie die Pipette senkrecht und geben Sie langsam 1 hängenden Tropfen Plasma (etwa 25 µL) in den Probenbereich, fügen Sie dann 2 Tropfen Puffer (etwa 80 µL) hinzu, und starten Sie den Kurzzeitwecker. Warten Sie mit dem Hinzufügen des jeweils nächsten Tropfens bis der vorherige vollständig aufgenommen wurde. Beachten Sie die Abbildung unten.
Für Venenpunktion-Vollblutproben:
• Halten Sie die Pipette senkrecht und geben Sie langsam 1 hängenden Tropfen Vollblut (etwa 25 µL) in den Probenbereich, fügen Sie dann 2 Tropfen Puffer (etwa 80 µL) hinzu, und starten Sie den Kurzzeitwecker. Warten Sie mit dem Hinzufügen des jeweils nächsten Tropfens bis der vorherige vollständig aufgenommen wurde. Beachten Sie die Abbildung unten.
Für Fingereinstich-Vollblutproben:
• Bei der Verwendung eines Kapillarröhrchens: Füllen Sie das Kapillarröhrchen und geben Sie etwa 25 µL der Fingereinstich-Vollblutprobe in den Probenbereich, fügen Sie dann 2 Tropfen Puffer (etwa 80 µL) hinzu, und starten Sie den Kurzzeitwecker. Warten Sie mit dem Hinzufügen des jeweils nächsten Tropfens bis der vorherige vollständig aufgenommen wurde. Beachten Sie die Abbildung unten.
• Bei der Verwendung von hängenden Tropfen: Erlauben Sie 1 hängenden Tropfen der Fingereinstich-Vollblutprobe (etwa 25 µL) in den Probenbereich der Testkassette zu fallen, fügen Sie dann 2 Tropfen Puffer (etwa 80 µL) hinzu, und starten Sie den Kurzzeitwecker. Warten Sie mit dem Hinzufügen des jeweils nächsten Tropfens bis der vorherige vollständig aufgenommen wurde. Beachten Sie die Abbildung unten.
- Warten Sie darauf, dass die farbige(n) Linie(n) erscheinen. Lesen Sie das Ergebnis nach 10 Minuten ab. Werten Sie das Ergebnis nicht nach mehr als 20 Minuten aus.
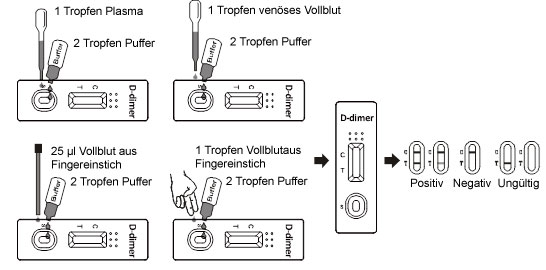
(Bitte beachten Sie die Abbildung oben)
AUSWERTUNG DER ERGEBNISSE
POSITIV:* Eine farbige Linie im Kontrolllinienbereich (C) und das Vorhandensein von einer oder mehr farbigen Linien im Testlinienbereich zeigt ein positives Ergebnis an. Dies bedeutet, dass die Konzentration von D-Dimer über der minimalen Nachweisgrenze liegt.
*HINWEIS: Die Farbintensität im Testlinienbereich schwankt in Abhängigkeit der Konzentration des D-Dimers in der Probe. Daher sollte jede Farbschattierung im Testlinienbereich als positiv betrachtet werden.
NEGATIV: Eine farbige Linie erscheint im Kontrolllinienbereich (C). Keine Linie erscheint im Testlinienbereich (T). Dies bedeutet, dass die Konzentration von D-Dimer unter der minimalen Nachweisgrenze liegt.
UNGÜLTIG: Es erscheint keine Kontrolllinie. Eine unzureichende Probemenge oder eine inkorrekte Durchführung sind die wahrscheinlichsten Gründe für das Fehlen der Kontrolllinie. Überprüfen Sie die Durchführung und wiederholen Sie den Test mit einer neuen Testkassette. Wenn das Problem weiterhin besteht, beenden Sie sofort die Verwendung des Testkits und setzen Sie sich mit Ihrem örtlichen Händler in Verbindung.
QUALITÄTSKONTROLLE
Der Test beinhaltet eine interne Verfahrenskontrolle. Eine rötliche Kontrolllinie in der Kontrollregion (C-Region) der Membran zeigt an, dass der Test richtig durchgeführt wurde. Im Rahmen einer guten Laborpraxis (GMP) wird der Einsatz externer Kontrollen zum Nachweis der ordnungsgemäßen Funktion des Tests empfohlen.
BESCHRÄNKUNGEN
- Ein negatives Ergebnis kann dazu beitragen mit einer sehr hohen Wahrscheinlichkeit disseminierte intravasale Gerinnungsstörung (DIC), tiefe Venenthrombose (TVT) und Lungenembolie (LE) auszuschließen. (1, 2)
- Wie bei allen diagnostischen Verfahren sollten die mit diesem Test erzielten Ergebnisse in Verbindung mit anderen, dem Arzt zur Verfügung stehenden Informationen, wie z.B. dem sog. „Wells Score“ für TVT bzw. LE genutzt werden. Insbesondere im Rahmen der Diagnose einer DIC, findet das Ergebnis des D-Dimer Tests Eingang in die Ermittlung des sog. „DIC Score“.(1)
- Die Sensitivität immunologischer Schnelltests bei Patienten mit mittlerer oder hoher klinischen Wahrscheinlichkeit einer Thrombose (hoher Wells Score) ist niedriger (negativer Vorhersagewert = 85,7 %), als bei Patienten mit niedriger klinischen Wahrscheinlichkeit (niedriger Wells Score; negativer Vorhersagewert = 99,5 %). Bei mittlerer und hoher klinischer Wahrscheinlichkeit wird daher eine sonografische Untersuchung unabhängig vom Ergebnis des Schnelltests angeraten.(3)
- Falsch negative Ablesewerte können auftreten, wenn die Probe entweder zu früh nach der Thrombusbildung entnommen wurde, wenn die Testdurchführung mehrere Tage verzögert wird oder wenn die Probe zu spät nach Eintritt des thromboembolischen Infarktes genommen wurde, denn die D-Dimer-Konzentration kann bereits nach einer Woche wieder auf normale Werte absinken. Außerdem kann eine Behandlung mit Antikoagulantien vor der Probenentnahme ein negatives Testergebnis verursachen, weil sie die Vergrößerung des Thrombus verhindert.(1, 4)
- Erhöhte D-Dimer-Werte trotz Behandlung mit Antikoagulantien weisen hingegen auf ein weiter bestehendes Thromboserisiko hin.(5)
- Ein positives Ergebnis ist kein Beweis für das Bestehen der oben genannten Erkrankungen. Falsch positive Ablesewerte können verschiedene Ursachen haben: Erkrankungen der Leber, Entzündung, bösartige Geschwülste, Trauma, Schwangerschaft,kürzlich durchgeführte Operationen sowie fortgeschrittenes Alter.(1,2)
- Es besteht die Möglichkeit, dass der Test kein Ergebnis bringt, wenn Vollblutprobeneine hohe Viskosität haben oder länger als einen Tag aufbewahrt wurden. In diesen Fällen sollte der Test mit einem neuen Test und einer frischen Probe desselben Patienten wiederholt werden.
ERWARTETE WERTE
Erhöhte D-Dimerkonzentrationen über dem allgemein anerkannten Grenzwert von 500 ng/ml FEU (f brinogen equivalent units) deuten auf eine aktive Fibrinolyse hin und wurden bei Patienten mit disseminierter intravasaler Gerinnungsstörung (DIC) tiefer Venenthrombose (TVT) und Lungenembolie nachgewiesen. Solche erhöhten Konzentrationen treten aber auch nach Operationen und Verletzungen, bei Sichelzellenanämie, Lebererkrankungen, schweren Infektionen, Sepsis, Entzündungen, bösartigen Tumorerkrankungen oder bei älteren Menschen auf. Die Konzentration von D-Dimer steigt auch in einer normalen Schwangerschaft.
LEISTUNGSCHARAKTERISTIKA
Sensitivität und Spezifität
Die D-Dimer Schnelltestkassette (Vollblut/ Plasma) wurde unter Verwendung von klinischen Proben mit einem führenden kommerziellen D-Dimer EIA Test ausgewertet. Die Ergebnisse zeigen, dass relativ zum führenden EIA Test die D-Dimer Schnelltestkassette (Vollblut/ Plasma) eine Sensitivität von >99.9% und eine Spezifität von 98.2% für D-Dimer zeigt.
D-Dimer Schnelltest vs. EIA
| Methode |
EIA |
Gesamtergebnis |
D-Dimer
Schnelltestkassette
(Vollblut/ Plasma) |
Ergebnisse |
Positiv |
Negativ |
| Positiv |
56 |
7 |
63 |
| Negativ |
0 |
387 |
387 |
| Gesamtergebnis |
56 |
394 |
450 |
Relative Sensitivität: 56/56=>99.9% (95%CI*: 94.8%~100.0%);
Relative Spezifität: 387/394=98.2% (95%CI*: 96.4%~99.3%);
Genauigkeit: (56+387)/ (56+7+387) =98.4%( 95%CI*: 96.8%~99.4%). *Konfidenzintervalle
Präzision
Intra-Assay
Die chargeninterne Präzision wurde durch die Verwendung von 15 Wiederholungen von fünf Proben bestimmt: D-Dimer Probengehalte von 0 ng/mL, 500 ng/mL, 1,000 ng/mL, 1,500 ng/mL und 3,000 ng/mL. Die Proben wurden insgesamt zu >99% korrekt erkannt.
Inter-Assay
Die Präzision zwischen den Chargen wurde durch 3 unabhängige Tests mit denselben fünf Proben bestimmt: 0 ng/mL, 500 ng/mL, 1,000 ng/mL, 1,500 ng/mL and 3,000 ng/mL D-Dimer. Drei unterschiedliche Chargen der D-Dimer Schnelltestkassette (Vollblut/Plasma) wurden unter Verwendung dieser Proben getestet. Die Proben wurden insgesamt zu >99% korrekt erkannt.
Kreuzreaktivität
Die D-Dimer Schnelltestkassette (Vollblut/ Plasma) wurde mit HBsAg,HBsAb,HBeAg,HBeAb,HBcAb,Syphilis,anti-HIV,anti-H.pylori,MONO,anti-CMV,anti-Rubella und anti-Toxoplasmosis positiv Proben getestet. Die Ergebnisse zeigten keine Kreuz-Reaktivität.
Störende Substanzen
Die folgenden potentiell störenden Substanzen wurden zu D-dimer negativen bzw. positiven Proben zugesetzt
Acetaminophen: 20 mg/dL
Acetylsalicylsäure: 20 mg/dL
Ascorbinsäure: 20mg/dL
Kreatin: 200 mg/dL
Bilirubin: 1,000mg/dL
Cholesterin: 800mg/dL
Coffein: 20 mg/dL
Gentisinsäure: 20 mg/dL
Albumin: 10,500mg/dL
Hämoglobin: 1,000 mg/dL
Oxalsäure: 600mg/dL
Triglyceride: 1,600mg/dL
Keine der Substanzen beeinträchtigte den Test in der untersuchten Konzentration.
Qualitätssicherung und Vorkommnisse
Sollten Sie den Eindruck eines Qualitätsmangels haben oder unklare oder ihrerseits falsch-positive oder falsch-negative Ergebnisse erhalten, bitten wir Sie, die betreffende Patientenprobe zurückzustellen und für einen Abruf für uns bereitzuhalten.
Bitte informieren Sie uns umgehend. Sie helfen uns dadurch die Sicherheit der Produkte und damit die Qualität zu gewährleisten.
LITERATUR
- Dempfl e, Carl-Erik (2005): Bestimmung des D-dimer-Antigens in der klinischen Routine, Deutsches Ärzteblatt Jg. 102, Heft 7, 18. Februar 2005: A428-A432.
- Fritscher, Claudia (2007): Bedeutung der D-dimer Untersuchung in der Diagnostik der tiefen Beinvenenthrombose,Labor Aktuell Nr.7/2007, 1-8.
- Brill-Edwards P., Lee A. (1999): D-dimer testing in the diagnosis of acute venous thromboembolism,Thrombosis and Heamostasis; 82(2): 688-94
- Blackwell Publishing Ltd. (2004): The diagnosis of deep vein thrombosis in symptomatic outpatients and the potential for clinical assessment and D-dimer assays to reduce the need for diagnostic imaging, British Journal of Haematology, 124, 15–25.
- Thomas, Lothar (2008): Labor und Diagnose (Indikation und Bewertung von Laborfunden für die medizinischen Diagnostik, TH-Books Verlagsgesellschaft mbH, Frankfurt/Main, 7.Auflage, 2008.
Abrechnung
| |
Nr. |
Preis in € |
| GOÄ |
3937
3938 |
13,64
20,98 |
bei med. Indikation.
Kassenleistung EBM |
32117
32212
32027 |
4,60
12,80
15,30 |
SYMBOLERKLÄRUNG
 |
Hersteller: |

Günter Keul GmbH
Von-Langen-Weg 10
D-48565 Steinfurt
Tel.: 02551/2097 Fax.: 02551/80883
Web: www.keul.de
|
(akt. 27.04.2016)
|
|