| |
Keul-o-test
Chlamydia Schnelltestkassette
für Abstrichproben
AMCT1

Verwendungszweck
Der Chlamydia-Trachomatis (CT) Schnelltest ist ein einfaches immunochromatographisches Assay für den schnellen, qualitativen Nachweis von CT in endocervikalen oder endourethralen Abstrichen
Das Erkennen hilft bei der Diagnose der Erkrankung die durch Bakterien hervorgerufen werden die zur Gattung Chlamydia gehören und bietet eine epidemiologische Information über diese Krankheit. Chlamydia sind kausative Erreger der Psittakose(eine Form der Lungenentzündung), Lymphogranuloma venereum (einer venerischen Erkrankung) und Trachom (einer chronischen Erkrankung des Auges und des Augenlids).
Vorsichtsmaßnahmen
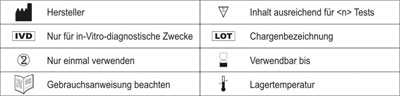
Die CT-Testkassette sollte bei Raumtemperatur 4-30°C (40-86°F) gelagert werden. Die Testkassette ist gegenüber Feuchtigkeit und Hitze empfindlich. Führen Sie den Test unverzüglich nach der Entnahme des Testkassette aus dem Folienbeutel durch. Verwenden Sie den Test nicht nach Ablauf des Verwendbarkeitsdatums.
Vorhandenes Material
Der Testkit enthält die folgenden Bestandteile um den Test durchzuführen:
- CT-Testkassette
- Einwegpipette
- Gebrauchsanleitung
- Tupfer für die Frau (Tupfer für den Mann müssen separat bestellt werden)
- Extraktionspuffer A und B
- Teströhrchen
- Ständer
Sammeln der Probe und Vorbereitung
a. Weibliche Patienten
Reiben Sie den Tupfer kräftig über die entzündete endourethrale Gewebe und die endocervicalen Zellen an der Wand des Zervixkanals. Weil Chlamydia intrazelluläre Organismen sind, muss zur ordnungsgemäßen Probenahme ein fester Kontakt mit der Wand des Zervixkanals erfolgen. Das Reiben beseitigt die endothelialen Zellen und erlaubt den Tupfer die Bakterien aufzunehmen. Eine unzureichende Probenahme führt zu einem beschwerlichen Ablesen und ungültigen Ergebnissen. Vaginale Proben sind nicht nützlich.
b. Männliche Patienten
- Führen Sie den Tupfer in die Harnröhre des Penis ein. Drehen Sie behutsam mit genügendem Druck, um die epithelialen Zellen zu beseitigen. Gestatten Sie dem Tupfer nach der Drehung einige Sekunden eingeführt zu bleiben.
- Entfernen Sie den Tupfer behutsam, wobei Sie den Kontakt mit anderen Oberflächen vermeiden.
Warnungen
- Nur für den in-vitro-diagnostischen Gebrauch
- Essen oder rauchen Sie nicht beim Umgang mit den Proben
- Tragen Sie Schutzhandschuhe beim Umgang mit den Proben. Waschen Sie sich die Hände anschließend sorgfältig.
- Vermeiden Sie Spritzer und Aerosolbildung.
- Beseitigen Sie Spritzer sorgfältig mit einem geeigneten Desinfektionsmittel.
- Reinigen und Entsorgen Sie alle Proben, Testbestandteile und potentiell kontaminierten Materialien so, als ob sie infektiöser Abfall sind in einem Behälter für biogefährliche Stoffe.
- Verwenden Sie den Test nicht, wenn die Folientasche oder die Versiegelung beschädigt ist.
Probenlagerung
Falls der Tupfer nicht sofort extrahiert wird, lagern Sie ihn vorzugsweise in einem Transportröhrchen gekühlt für bis zu 5 Tage. Nicht einfrieren. Tupfer können unter Umgebungsbedingungen zum Ort der Testdurchführung transportiert werden. Transportmedien sollten nicht verwendet werden.
Probenvorbereitung
- Bringen Sie vor dem Test alle Proben auf Raumtemperatur.
- Geben Sie 6 Tropfen des Extraktionspuffers A in ein Teströhrchen. Geben Sie den Probentupfer in das Röhrchen und rühren Sie kräftig für etwa 15 Sekunden um die Reagenzien zu mischen. Inkubieren Sie die Mischung bei Raumtemperatur für eine Minute mit dem Tupfer im Röhrchen.
-
Geben Sie 6 Tropfen des Extraktionspuffers B in das Teströhrchen.
- Rühren Sie mit dem Tupfer für 15 Sekunden, entnehmen Sie dann den Tupfer, wobei Sie durch Drehen und Drücken des Faserteils gegen die Wand des Röhrchens, so viel wie möglich Flüssigkeit herauspressen. Entsorgen Sie den Tupfer. Mischen Sie den Inhalt des Röhrchens durch behutsames Schwenken. Der Tupferextrakt kann sofort getestet werden oder bis zu 3 Stunden bei Raumtemperatur verbleiben, ohne dass Dies die Testergebnisse beeinträchtigt.
Durchführung des Tests
- Entnehmen Sie die Testkassette aus dem Folienbeutel und legen Sie sie auf eine flache, trockene Oberfläche.
- Halten Sie die Einwegpipette über die Testkassette und geben Sie langsam 2 hängende Tropfen der extrahierten Probe in die Probeaufnahmevertiefung (Abbildung 1). Warten Sie mit dem Hinzufügen des zweiten Tropfens bis der erste vollständig aufgenommen wurde.
- Wenn der Test beginnt abzulaufen, sehen Sie eine Purpurfärbung, die sich durch das Ergebnisfenster in der Mitte der Testkassette bewegt.
- Werten Sie die Testergebnisse nach 15 Minuten aus. Nehmen Sie nach mehr als 15 Minuten keine Auswertung mehr vor.
Vorsicht: Die oben angegebene Auswertungszeit beruht auf einem Ablesen der Testergebnisse bei Raumtemperatur von 15 bis 30°C. Wenn Ihre Raumtemperatur deutlich niedriger als 15°C ist, dann sollte die Auswertungszeit entsprechend verlängert werden.
Auswertung des Test
- Wenn der Test beginnt abzulaufen, erscheint eine Farblinie im linken Teil des Ergebnisfensters um anzuzeigen, dass der Test ordnungsgemäß funktioniert. Diese Linie ist die Kontrolllinie (C).
- Der rechte Teil des Ergebnisfensters zeigt das Testergebnis an. Wenn eine weitere Farblinie im rechten Teil des Ergebnisfensters erscheint, ist diese Linie die Testlinie (T).
Positives Ergebnis: Zwei Farblinien
Das Vorhandensein von zwei Farblinien („T“-Linie und „C“-Linie) im Ergebnisfenster zeigen, ungeachtet welche Linie zuerst erscheint, ein positives Ergebnis an (Abbildung 2). Hinweis: Allgemein gilt, je höher der Analytgehalt in der Probe ist, desto stärker wird die „T“-Linie sein. Wenn der Analytgehalt in der Probe nahe aber noch innerhalb der Empfindlichkeitsgrenze des Tests ist, , wird die Färbung der „T“-Linie sehr schwach sein.
Negatives Ergebnis: Eine Farblinie
Das Vorhandensein nur einer purpurnen Farblinie im Ergebnisfenster zeigt ein negatives Ergebnis an (Abbildung 3).
Ungültiges Ergebnis
Wenn nach der Durchführung des Tests keine Linie im Ergebnisfenster sichtbar ist, ist das Ergebnis als ungültig zu betrachten (Abbildung 4). Die Anleitung wurde nicht korrekt befolgt oder der Test wurde beschädigt. Es wird empfohlen die Probe erneut zu testen.
Hinweis: Ein positives Ergebnis, welches sich nach 10 bis 20 Minuten eingestellt hat, wird sich nicht mehr ändern. Trotzdem sollte der Teste nicht nach mehr als 30 Minuten ausgewertet werden, um falsche Ergebnisse zu vermeiden.
Beschränkungen des Tests
Der Test ist auf den Nachweis von Chlamydia Trachomatis in Abstrichproben beschränkt. Obgleich der Test sehr genau bei Nachweis von CT ist, können selten falsche Ergebnisse vorkommen. Andere klinisch verfügbare Tests sind dann erforderlich, wenn fragwürdige Ergebnisse erhalten wurden. Ebenso wie bei allen diagnostischen Tests sollte eine abschließende klinische Diagnose nicht nur auf den Ergebnissen eines einzelnen Tests beruhen, sondern sollte vom Arzt nur nach Auswertung aller klinischen und Laborbefunde erfolgen.
Spezifität und Interferenzstudie
Die Kreuzreaktivität mit anderen Organismen wurde mit einer Suspension von 1×10^7 CFU/ml (CFU- koloniebildende Einheit) untersucht und ergab negative Chlamydia-Ergebnisse. Staphylococcus aureus wurde mit 1×10^6 Zellen/Test untersucht und erbrachte ebenso negative Ergebnisse.
Die getesteten Organismen sind nachfolgend aufgeführt:
- Candida abbicans
- Neisseria lactamica Saccharomyces cerevisiae
- Eschericha coli
- Neisseria meningitides Streptococcus faecalis
- Gardnerella vaginalis
- Neissera meningitidi
- Streptococcus Gruppe A
- Streptococcus Gruppe B
- Klebsiella pneumonia
- Proteus vulgaris
- Streptococcus pneumoniae
- Neisseria gonorrhoeae
- Pseudomonas aeruginosa
Literatur
- Bibbo M and Wied GL, „Inflammation Reaction and Microbiology of the Female Productive Tract,“ Compendium on Diagnostic Cytology, Wied GL, Keebler CM, Koss LG, et al, eds, Chicago, IL: Tutorials of Cytology, 1992,63-8.
- Ehert JM and Judson FN, “Genital Chlamydia Infections,” Clin Lab med, 1989,9(3): 481-500.
- Gay JD, Donalson LD, and Goellner JR, “False-Negative results in Cervical Cytologic Studies,” Acta Cytol, 1985, 29:1043-6.
- Gupta PK, „Microbiology, Inflammation, and Viral Infection,“ Comprehensive Cytopathology, Ist ed, Bibbo M, ed, Philadelphia, PA: WB Saunders Co, 1991, 115-52.
- Luff RD, ‚“The Bethesda System for Reporting Cervical/Vaginal Diagnosis,” Acta Cytol, 1993, 37(2): 115-24. Maguire NC, „Current Use of the Papanicolaou Class System in Gynecologic Cytology,“ Diagn Cytopathol, 1988. 4: 169-76.
- Miettinen A, Heinonen PK, Teisala K, et al, „Antigen-Specific Serum Antibody Response to Chlamydia trachomalis in Patients With Pelvic Inflammatory Disease,“ J Clin Pathol, 1990, 43(9):758-61.
- Schachter J, „Chlamydiae,“ Manuel of Clinical Laborotory Immunology, 4th ed, Vol 2, Chapter 96, Rose NR, Conway de Macario E, Fahey JL, et al, eds. Washington, DC: American Society for Microbiology, 1992,661-6,
QUALITÄTSSICHERUNG UND VORKOMMNISSE
Sollten Sie den Eindruck eines Qualitätsmangels haben oder unklare oder ihrerseits falsch-positive oder falsch-negative Ergebnisse erhalten, bitten wir Sie, die betreffende Patientenprobe zurückzustellen und für einen Abruf für uns bereitzuhalten.
Bitte informieren Sie uns umgehend. Sie helfen uns dadurch die Sicherheit der Produkte und damit die Qualität zu gewährleisten.
 0843 0843
| Hersteller: |
Ameritech Diagnostic Reagents (Jiaxing) Co., Ltd
K4-2 Science Technology Garden
Economic Development Zone, Tongxiang
Zhejiang Province, 314500
P. R. China |
akt. 04.01.2016
|
|