Ein Schnelltest für die Diagnose von Entzündungszuständen durch den qualitativen Nachweis von Serum-Amyloid A (SAA) und C-reaktivem Protein in Vollblut, Serum oder Plasma. Nur für professionelle In-vitro-Diagnostik.
>> EINSATZZWECK
Die SAA und CRP Combo Schnelltestkassette (Vollblut / Serum / Plasma) ist ein schneller chromatographischer Immunoassay zum qualitativen Nachweis von humanem SAA und CRP in Vollblut, Serum oder Plasma als Hilfe bei der Diagnose von Entzündungszuständen. Der Grenzwert für SAA beträgt 10 μg / ml und der Cut-off für CRP beträgt 10 μg / ml.
>>Zusammenfassung
Serum-Amyloid A (SAA) -Proteine sind eine Familie von Apolipoproteinen, die mit hochdichtem Lipoprotein (HDL) im Plasma assoziiert sind. Verschiedene Isoformen von SAA werden konstitutiv (konstitutive SAAs) auf verschiedenen Ebenen oder als Reaktion auf inflammatorische Stimuli (akute Phase SAAs) exprimiert. Diese Proteine werden hauptsächlich von der Leber produziert.1 Die Konservierung dieser Proteine in Invertebraten und Wirbeltieren legt nahe, dass SAAs bei allen Tieren eine sehr wichtige Rolle spielen.2
Akutphasen-Serum-Amyloid-A-Proteine (A-SAAs) werden während der akuten Phase der Entzündung sezerniert. Diese Proteine haben mehrere Rollen, einschließlich des Transports von Cholesterin in die Leber zur Sekretion in die Galle, die Rekrutierung von Immunzellen zu entzündlichen Stellen und die Induktion von Enzymen, die die extrazelluläre Matrix abbauen.
Serum-Amyloid A (SAA) ist auch ein Akutphasenmarker, der schnell reagiert. Ähnlich wie bei CRP steigen die Werte der SAA in der akuten Phase innerhalb von Stunden nach dem Entzündungsstimulus an, und das Ausmaß der Zunahme kann größer sein als das von CRP. Relativ triviale Entzündungsreize können zu SAA-Reaktionen führen. Es wurde vorgeschlagen, dass die SAA-Spiegel besser mit der Krankheitsaktivität bei frühen entzündlichen Gelenkerkrankungen korrelieren als ESR und CRP. Obwohl sie hauptsächlich von Hepatozyten produziert werden, zeigen neuere Studien, dass SAA auch von Adipozyten produziert wird und ihre Serumkonzentration mit dem Body-Mass-Index assoziiert ist.3
C-reaktives Protein (CRP) ist ein ringförmiges (ringförmiges), pentameres Protein, das im Blutplasma gefunden wird und dessen Spiegel als Reaktion auf eine Entzündung ansteigt. Es ist ein akutphasiges Protein hepatischen Ursprungs, das nach Interleukin-6-Sekretion durch Makrophagen und T-Zellen zunimmt. Seine physiologische Rolle besteht darin, an Lysophosphatidylcholin zu binden, das auf der Oberfläche von toten oder sterbenden Zellen (und einigen Arten von Bakterien) exprimiert wird, um das Komplementsystem über C1q.4 zu aktivieren CRP spielt eine Rolle bei der angeborenen Immunität durch Bindung an das Phosphocholin, das auf der Oberfläche von toten oder sterbenden Zellen und einigen Bakterien exprimiert wird. Dies aktiviert das Komplementsystem, fördert die Phagozytose durch Makrophagen, die nekrotische und apoptotische Zellen und Bakterien freisetzt.
>>Prinzip
Die SAA und CRP Combo Schnelltestkassette besteht aus zwei Teilen. Ein Teil ist für SAA und ein anderer ist für CRP. Beide sind qualitative
Festphasen-Zwei-Stellen-Sandwich-Immunoassays zum Nachweis von Zielanalyten, d. H. SAA oder CRP, in Vollblut, Serum oder Plasma. In zwei separaten Abschnitten unten werden die Prinzipien für beide beschrieben.
Für SAA
Die Membran ist auf dem Testlinienbereich der Kassette mit Anti-SAA-Antikörpern vorbeschichtet. Während der Tests reagiert SAA, wenn es in der Probe (Vollblut, Serum oder Plasma) oberhalb der Cut-Off-Konzentration vorhanden ist, mit kolloidalen Gold-konjugierten Anti-SAA-Antikörpern. Der Komplex wandert auf der Membran chromatographisch durch Kapillarwirkung nach oben, um mit Anti-SAA-Antikörpern auf der Membran zu reagieren und eine farbige Linie zu erzeugen. Das Vorhandensein dieser farbigen Linie in der Testregion zeigt ein positives Ergebnis an, während ihre Abwesenheit ein negatives Ergebnis anzeigt. Um als Verfahrenskontrolle zu dienen, erscheint immer eine farbige Linie im Bereich der Kontrolllinie, die anzeigt, dass das richtige Volumen der Probe hinzugefügt wurde und Membran-Dochtwirkung aufgetreten ist.
Für CRP
Die Membran ist im Bereich der Testlinie der Kassette mit Anti-CRP-Antikörpern vorbeschichtet. Während der Testung reagiert CRP, falls vorhanden, die Probe (Vollblut, Serum oder Plasma) oberhalb der Cut-Off-Konzentration mit den kolloidalen Gold-konjugierten Anti-CRP-Antikörpern. Die Mischung wandert auf der Membran chromatographisch durch Kapillarwirkung nach oben, um mit anti-CRP-Antikörpern auf der Membran zu reagieren und eine farbige Linie zu erzeugen. Das Vorhandensein dieser farbigen Linie in der Testregion zeigt ein positives Ergebnis an, während ihre Abwesenheit ein negatives Ergebnis anzeigt. Um als Verfahrenskontrolle zu dienen, erscheint immer eine farbige Linie im Bereich der Kontrolllinie, die anzeigt, dass das richtige Volumen der Probe hinzugefügt wurde und Membran-Dochtwirkung aufgetreten ist.
>>Reagenzien
Die SAA- und CRP-Combo-Schnelltestkassette enthält kolloidalen Gold-konjugierten Anti-SAA-SAA-Antikörper, der auf der Membran zusammen mit kolloidalem Gold-konjugiertem Anti-CRP-Antikörper und CRP-Antikörper beschichtet auf der Membran aufgebracht ist.
>>Vorsichtsmaßnahmen
• Nur für professionelle In-vitro-Diagnostik. Verwenden Sie nicht nach Ablauf des Verfallsdatums.
• Essen, trinken oder rauchen Sie nicht in dem Bereich, in dem die Proben oder Kits gehandhabt werden.
• Verwenden Sie den Test nicht, wenn der Beutel beschädigt ist.
• Behandeln Sie alle Proben so, als ob sie infektiöse Agenzien enthalten. Beachten Sie bei allen Verfahren die festgelegten Vorsichtsmaßnahmen gegen mikrobiologische Gefahren und befolgen Sie die Standardverfahren für die ordnungsgemäße Entsorgung von Proben.
• Tragen Sie bei der Untersuchung von Proben Schutzkleidung wie Labormäntel, Einweghandschuhe und Augenschutz.
• Der verwendete Test sollte entsprechend den örtlichen Vorschriften entsorgt werden.
• Feuchtigkeit und Temperatur können die Ergebnisse beeinträchtigen.
>>LAGERUNG UND STABILITÄT
Im verschlossenen Beutel entweder bei Raumtemperatur oder gekühlt (2-30 ° C) aufbewahren. Der Test ist bis zum auf dem versiegelten Beutel aufgedruckten Verfallsdatum stabil. Der Test muss bis zur Verwendung in dem versiegelten Beutel bleiben. NICHT EINFRIEREN. Verwenden Sie nicht nach dem Ablaufdatum.
>>PROBENENTNAHME UND -VORBEREITUNG
Vorbereitung
Stellen Sie vor der Durchführung des Tests sicher, dass alle Komponenten auf Raumtemperatur (15-30 ° C) gebracht werden.
1. Nehmen Sie ein Röhrchen mit Pufferlösung aus dem Kit. Dokumentieren Sie den Namen oder die ID des Patienten darauf. Schrauben Sie die Kappe ab.
Probenentnahme
2. Sammeln Sie die Probe gemäß Standardverfahren.
• Proben nicht längere Zeit bei Raumtemperatur liegen lassen. Serum- und Plasmaproben können bis zu 3 Tage lang bei 2-8 ° C gelagert werden. Bei längerer Lagerung sollten Proben unter -20 °C aufbewahrt werden. Vollblut, das durch Venenpunktion entnommen wurde, sollte bei 2-8 ° C gelagert werden, wenn der Test innerhalb von 2 Tagen nach der Entnahme verwendet werden soll. Frieren Sie keine Vollblutproben ein. Vollblut, das mit dem Fingerstäbchen entnommen wurde, sollte sofort getestet werden.
• Proben vor dem Test auf Raumtemperatur bringen. Gefrorene Proben müssen vor dem Test vollständig aufgetaut und gemischt werden. Wiederholtes Einfrieren und Auftauen von Proben vermeiden.
• EDTA K2, Heparin-Natrium, Citrat-Natrium und Oxalat-Kalium können als Antikoagulanzien verwendet werden. Die Proben, die mit diesen Antikoagulantien gesammelt wurden, müssen auch dem gleichen Schritt der Verdünnung mit Puffer folgen.
Probenverdünnung / Probenstabilität
3. Verabreichen Sie die mit Blut gefüllte End-to-End-Kapillare in den Plastikschlauch mit Verdünnungspuffer. Alternativ können die 10 μl Probe direkt mit der Mikropipette in den Puffer gegeben werden.
4. Schließen Sie das Röhrchen und schütteln Sie die Probe ca. 10 Sekunden lang kräftig, um Probe und Verdünnungspuffer gut zu vermischen.
5. Lassen Sie die verdünnte Probe für 1 Minute homogenisieren. Schütteln Sie es während dieser Zeit nicht. 6. Die Probe kann sofort verwendet oder für bis zu 8 Stunden gelagert werden.
>>Materialien
Materialien zur Verfügung gestellt
• Testkassetten • Kunststofftuben mit Puffer • Kapillaren • Packungsbeilage • Tropfer
Benötigte, aber nicht mitgelieferte Materialien
• Timer• Lanzetten • Probensammelbehälter • Zentrifuge
>>Gebrauchsanweisung
Vor Gebrauch Proben, Proben, Puffer und / oder Kontrollen auf Raumtemperatur (15-30 ° C) bringen.
1. Nehmen Sie die Testkassette aus dem versiegelten Beutel und legen Sie sie auf eine saubere, ebene Oberfläche.
—Für beste Ergebnisse sollte der Test innerhalb einer Stunde durchgeführt werden.—
2. Öffnen Sie das Röhrchen mit der verdünnten Probe. Bringen Sie 3 Tropfen der verdünnten Probe (ca. 120 μl) in jede Probenvertiefung (S). Starten Sie den Timer.
3. Warten Sie, bis die farbigen Linien angezeigt werden. Das Ergebnis sollte nach 5 Minuten abgelesen werden.
Interpretieren Sie die Ergebnisse nicht nach 10 Minuten.
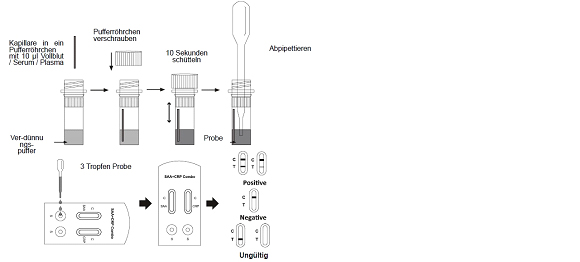
>>Interpretation der Ergebnisse
POSITIV: * Zwei Linien erscheinen. Eine farbige Linie sollte in der Kontrolllinienregion (C) sein und eine andere
sichtbare farbige Linie sollte in der Testlinienregion (T) sein.
* HINWEIS: Die Intensität der Farbe in der Testlinienregion (T) hängt von der Konzentration des SAA-Antigens
und oder CRP-Antigens in der Probe ab. Daher sollte jeder Farbton in der Testlinienregion (T) als
positiv betrachtet werden.
NEGATIV: Eine farbige Linie erscheint in der Kontrolllinienregion (C). In der Testlinienregion (T) erscheint
keine Linie.
Ungültig: Steuerzeile wird nicht angezeigt. Unzureichendes Probenvolumen oder falsche Verfahrenstechniken sind
die wahrscheinlichsten Gründe für das Versagen der Kontrolllinie. Überprüfen Sie den Vorgang und
wiederholen Sie den Test mit einem neuen Test. Wenn das Problem weiterhin besteht, brechen Sie die Verwendung des Testkits ab und wenden Sie sich an die Günter Keul GmbH oder Ihren lokalen Händler.
>>Qualitätskontrolle
Interne Verfahrenskontrollen sind im Test enthalten. Die Kontrolllinie, die in den Kontrollregionen erscheint, wird als eine interne positive Verfahrenskontrolle angesehen, die ein ausreichendes Probenvolumen und eine korrekte
Verfahrenstechnik bestätigt.
Externe Steuerelemente sind nicht im Lieferumfang dieses Kits enthalten. Es wird empfohlen, positive und negative Kontrollen als gute Laborpraxis zu testen, um das Testverfahren zu bestätigen und die ordnungsgemäße Testleistung zu überprüfen.
>>Einschränkungen
1. Die SAA und CRP Combo Schnelltestkassette (Vollblut / Serum / Plasma) ist für die professionelle In-vitro-Diagnostik bestimmt und sollte nur zum qualitativen Nachweis von Serum-Amyloid-A-Protein und C-reaktivem Protein verwendet werden. 2. Die SAA- und CRP-Combo-Schnelltestkassette (Vollblut / Serum / Plasma) zeigt nur das Vorhandensein von Serum-Amyloid-A-Protein und / oder CRP-Antigen in der Probe an und solltenicht als einziges Kriterium zur Beurteilung entzündlicher Zustände verwendet werden.
3. Wie bei allen diagnostischen Tests müssen alle Ergebnisse zusammen mit anderen klinischen Informationen, die dem Arzt zur Verfügung stehen, berücksichtigt werden.
4. Eine schwache Linie kann auftreten, wenn die Konzentration des Serum-Amyloid-A-Proteins oder CRP-Antigens in der Probe nahe bei 10 ug / ml lag. 5. Der Hämatokritwert des Vollbluts sollte zwischen 25% und 65% liegen.
>>Erwartete Werte
In einem normalen gesunden Individuum ohne ausgeprägte Entzündung sollte der Spiegel für SAA und CRP unter 10μg/ml betragen.
>>Leistungsmerkmale
Klinische Sensitivität, Spezifität und Gesamtgenauigkeit
Die SAA und CRP Combo Schnelltestkassette (Vollblut / Serum / Plasma) wurde mit führenden kommerziellen Immunturbidimetrie (ITM)-Tests verglichen; Die Ergebnisse zeigen, dass SAA- und CRP-Schnelltestkassetten (Vollblut / Serum / Plasma) eine hohe Sensitivität und Spezifität aufweisen.
SAA Keul-o-test
|
Methode
|
Test
|
Gesamt-ergebnis
|
|
SAA Schnelltest- kassette (Vollblut/Serum/
Plasma)
|
Ergebnisse
|
Positiv
|
Negativ
|
|
Positiv
|
97
|
4
|
101
|
|
Negativ
|
2
|
233
|
235
|
|
Gesamtergebnis
|
99
|
237
|
336
|
Relative Sensitivität: 97.9% (97.5%CI*: 92.9%-99.8%)
Relative Spezifität: 98.3% (95%CI*: 95.7%-99.5%)
Genauigkeit: 98.2% (95%CI*: 96.2%-99.3%) *Konfidenzintervall
CRP Keul-o-test
|
Methode
|
Test
|
Gesamt-ergebnis
|
|
CRP
Schnelltest- kassette (Vollblut/Serum/ Plasma)
|
Ergebnisse
|
Positiv
|
Negativ
|
|
Positiv
|
103
|
3
|
106
|
|
Negativ
|
2
|
247
|
249
|
|
Gesamtergebnis
|
105
|
250
|
355
|
Relative Sensitivität: 98.1% (97.5%CI*: 93.3%-99.8%)
Relative Spezifität: 98.8% (95%CI*: 96.5%-99.8%)
Inter-Assay
Für SAA wurde die Interventions-Laufpräzision unter Verwendung der gleichen Proben von negativer 10 μg / ml SAA-, 40 μg / ml SAA- und 100 μg / ml SAA-Standardprobe in 3 unabhängigen Assays bestimmt. Drei verschiedene Chargen der SAA-Schnelltestkassette (Vollblut / Serum / Plasma) wurden über einen Zeitraum von 3 Tagen mit negativen, schwach positiven und hoch positiven Proben getestet. Die Proben wurden zu 99% korrekt identifiziert.
Für CRP wurde die Durchlauf-Präzision bestimmt, indem dieselben Proben von negativem, 10 ug / ml CRP, 40 ug / ml CRP und 80 ug / ml CRP-Standardprobe in 3 unabhängigen Assays verwendet wurden. Drei verschiedene Chargen der CRP-Schnelltestkassette (Vollblut / Serum / Plasma) wurden über einen Zeitraum von 3 Tagen mit negativen, schwach positiven und hoch positiven Proben getestet. Die Proben wurden zu 99% korrekt identifiziert.
Kreuzreaktivität
Die SAA und CRP Combo Schnelltestkassette (Vollblut / Serum / Plasma) wurde getestet mit HBsAg, Anti-HIV, Anti-HCV, Anti-Syphilis, Rheumafaktor (RF), Anti-H. Pylori, Anti-CMV-IgG, Anti-Rubella-IgG und Anti-TOXO-IgG-positive Proben. Die
Ergebnisse zeigten keine Kreuzreaktivität
Störsubstanzen
Die folgenden potentiell störenden Substanzen wurden zu SAA / CRP-negativen und positiven Proben hinzugefügt.
|
Acetaminophen:
20 mg / dL
|
|
Koffein:
20 mg / dL
|
|
Acetylsalicylsäure:
20 mg / dl
|
|
Gentisinsäure: 20 mg / dl
|
|
Ascorbinsäure:
2 g / dl
|
|
Albumin:
2 g / dl
|
|
Kreatin:
200 mg / dl
|
|
Hämoglobin 1000 mg / dl
|
|
Bilirubin:
1 g / dL
|
|
Oxalsäure:
60 mg / dl
|
Keine der Substanzen in der getesteten Konzentration beeinträchtigte den Test.
>> LITERATURVERZEICHNIS
1. Uhlar CM, Whitehead AS (Oktober 1999). „Serum Amyloid A, der Hauptreaktant der Akutphase der Wirbeltiere“. Europäisches Journal für Biochemie.
2. Manley PN, Ancsin JB, Kisilevsky R (2006). „Schnelles Recycling von Cholesterin: die gemeinsame biologische Rolle von C-reaktivem Protein und Serumamyloid A“. Medizinische Hypothesen.
3.