| |
Keul-o-test®
C.Diff Toxin A/B Combo Testkassette für Stuhlproben
Bestellnummer: KGST203
DIMDI Reg.-Nr.: DE/CA22/1116-134-IVD
Verwendungszweck
Der Keul-o-test® C. difficile Toxin A/B Combo Test dient zum qualitativen Nachweis von Clostridium Difficile Toxinen A und/oder B in menschlichen Stuhlproben. Dieser Test ist eine Hilfe bei der Diagnose einer C. difficile-verwandten Krankheit (CDAD) bei Patienten mit Symptomen von CDAD.
Wirkungsweise
Der Keul-o-test® C. difficile Toxin A/B ist ein qualitativer Test der immunochromatographische Technologie verwendet. Der Testaufbau beruht auf einer mehrlagigen Immunoassay-Nitrozellulose in einer Kombinationskassette zum Nachweis von Toxin A und Toxin B. Der Testvorgang beinhaltet die Bildung von C. difficile Toxin A oder Toxin B aus der Stuhlprobe des Patienten, die zur Färbung von Partikeln führt, die an einen monoclonalen Antikörker gegen Toxin B oder einem polyclonalen Antikörper gegen Toxin A konjugiert sind. Wenn Toxin A und/oder B in der Probe vorhanden ist, führt dies zu einem teilweisen Immunkomplex mit den antikörper-konjugierten farbigen Partikel.
Lagerung und Stabilität
Der Keul-o-test® C.difficile-Toxin-A/B sollte bei Raumtemperatur oder 2-30° C (36-86° F) gelagert werden. Die Testkassette ist sowohl gegenüber Feuchtigkeit als auch Hitze empfindlich. Führen Sie den Test sofort aus, nachdem Sie die Testkassette aus der Folientasche entnommen haben. Verwenden Sie ihn nicht nach Ablauf des Haltbarkeitsdatums.
Warnungen
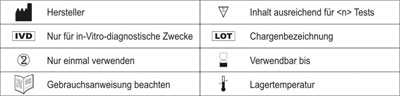
- Nur für den in-vitro-diagnostischen Gebrauch..
- Essen und rauchen Sie nicht beim Umgang mit den Proben.
- Tragen Sie Schutzhandschuhe beim Umgang mit den Proben. Waschen Sie sich die Hände anschließend gründlich.
- Vermeiden Sie Spritzer oder Aerosolbildung.
- Beseitigen Sie Spritzer gründlich mit einem geeigneten Desinfektionsmittel.
- Dekontaminieren und entsorgen Sie alle Proben, den Test und potentiell verunreinigte Materialien so als ob sie infektiöser Abfall wären in einem Gefahrenbehälter.
- Verwenden Sie den Test nicht, wenn der Folienbeutel oder die Versiegelung beschädigt ist.
Zubehör:
- Extraktionsröhrchen (vorhanden)
Probenahme
- Für diesen Test sollten nur Stuhlproben verwendet werden. Diese können vom Toilettenpapier gesammelt oder in einem sauberen Behälter aufgefangen werden. Die Proben sollten vor einer Verunreinigung mit Toilettenwasser geschützt werden.
- Schrauben Sie die Spitze des Probenahmeröhrchens ab und verwenden Sie den Probenahmesammelstab um die Stuhlprobe zu nehmen, indem Sie den Stab zufällig an 3 unterschiedlichen Stellen in die gleiche Stuhlprobe eintauchen. (Abb. 1)
- Führen Sie den Probesammelstab mit der Probe zurück in das Probesammelröhrchen und schrauben Sie es fest zu. Schütteln Sie es sehr gut.
- Die gesammelte Probe kann bei 2 bis 8° C für 3 Tage gelagert werden.
Testdurchführung
- Entnehmen Sie die Testkassette aus dem Folienbeutel und legen Sie sie auf eine ebene, trockene Oberfläche.
- Falls die Stuhlprobe gekühlt ist, dann bringen Sie das Probesammelröhrchen auf Raumtemperatur. Schütteln Sie dann das Röhrchen einige Male.
- Halten Sie das Probensammelröhrchen so, dass die Spitze oben ist, brechen dann die Spitze des Probensammelröhrchens ab und geben 3 hängende Tropfen der extrahierten Probe in jede der Probenaufnahmevertiefungen. (Abb2) Warten Sie bei der Zugabe der Tropfens stets so lange, bis der vorangegangene Tropfen vollständig aufgenommen wurde.
- Wenn der Test beginnt abzulaufen, werden Sie eine violette Farbfront sehen, die sich durch das Ergebnisfenster in der Mitte der Testkassette bewegt.
- Werten Sie das Testergebnis nach 9 bis 10 Minuten aus. Nehmen Sie nach mehr als 10 Minuten keine Auswertung mehr vor.
Achtung: Die oben angegebene Auswertungszeit beruht auf einem Ablesen der Testergebnisse bei einer Raumtemperatur von 15 bis 30° C. Wenn Ihre Raumtemperatur deutlich niedriger als 15° C ist, dann sollte die Auswertungszeit entsprechend verlängert werden
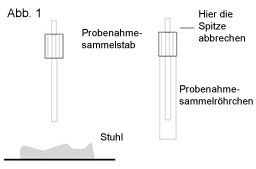 Abb. 2 Abb. 2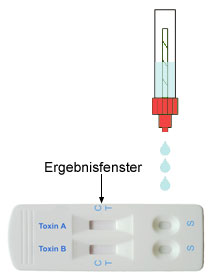
|
|
| Abb. 3 |
Abb. 4 |
Abb. 5 |
Abb. 6 |
Abb. 7 |
Abb. 8 |
positiv
|
positiv |
positiv |
negativ |
ungültig |
ungültig |
Auswertung des Tests
- Eine Farblinie erscheint im linken Bereich des Ergebnisfensters um anzuzeigen, dass der Test ordnungsgemäß durchgeführt wurde. Diese Linie ist die Kontrolllinie.
- Wenn C.Diff Toxin-A in der Probe nachgewiesen wurde, erscheint eine Farblinie an der mit „T“ gekennzeichneten Stelle des Tonin-A Bereiches (gekennzeichnet durch die Aufschrift „Toxin-A“) des Ergebnisfensters.
- Wenn C.Diff Toxin-B in der Probe nachgewiesen wurde, erscheint eine Farblinie an der mit „T“ gekennzeichneten Stelle des Tonin-B Bereiches (gekennzeichnet durch die Aufschrift „Toxin-B“) des Ergebnisfensters.
Positives Ergebnis: Das Vorhandensein der „C“ Farblinie in Verbindung mit einer oder beiden sichtbaren Testlinien „T“ des Toxin-A bzw. Toxin-B Bereiches (gleich welche Linie zuerst erscheint), zeigt ein positives Ergebnis an. (Abb. 3, 4, 5).
Negatives Ergebnis: Wenn nur die „C“ Farblinie im Ergebnisfenster in beiden, dem Toxin-A und dem Toxin-B Bereich vorhanden ist, dann zeigt dies ein negatives Ergebnis an. (Abb. 6)
Ungültiges Ergebnis: Wenn nach der Durchführung des Tests keine Farblinie oder keine „C“-Farblinie im Ergebnisfenster sichtbar ist, dann ist der Test als ungültig zu betrachten. Die Anleitung könnte nicht korrekt befolgt worden sein, oder der Test war beschädigt. Es wird empfohlen die Probe erneut zu testen.. (Abb. 7 und 8)
Hinweis: Wenn sich ein positives Ergebnis eingestellt hat (nach 10 Minuten), wird sich dieses Ergebnis nicht ändern. Trotzdem sollte, um jegliche falsche Ergebnisse zu vermeiden, das Testergebnis nicht nach mehr als 10 Minuten ausgewertet werden.
Leistungsmerkmale:
Sensitivität und Spezifität
In einer internen Studie mit 300 Teilnehmern wurde eine relative Sensitivität des Keul-o-test® C.Diff von 88,4%/ und eine relative Spezifität von 97,2% im Vergleich mit einem anderen kommerziell erhältlichen Test ermittelt. Die analytische Sensitivität ist 15ng/ml(Toxin-A) und 40ng/ml (Toxin-B).
Kreuzreaktivität
Die folgenden Organismen wurden mit 1.0 x 107 Organismen je Test untersucht und alle bezüglich der Combo-Testkassette als negative befunden. Es wurden keine schleimbildenden Stämme getestet.
|
Aeromonas hydrophila
|
Clostridium perfringens
|
Giardia lamblia
|
|
Bacillus cereus
|
Clostridium septicum
|
2
|
|
Bacillus subtilis
|
Clostridium sordellii
|
Helicobacter pylori
|
|
Bacteroides fragilis
|
Clostridium sporogenes
|
Klebsiella pneumoniae
|
|
Campylobacter coli
|
Clostridium tetani
|
Peptostreptococuss anaerobius
|
|
Campylobacter fetus
|
Cryptosporidium parvum
|
Porphyromonas asaccharolytica
|
|
Campylobacter jejuni
|
Enterobacter aerogenes
|
Proteus vulgaris
|
|
Candida albicans
|
Enterobacter cloacae
|
Pseudomonas aeruginosa
|
|
Clostridium difficile (nicht toxigen)
|
Enterococcus faecalis
|
Salmonella typhimurium
|
|
Clostridium beijerinckii
|
Escherichia coli
|
Serratia liquefaciens
|
|
Clostridium haemolyticum
|
Escherichia coli sero:0157
|
Shigella dysenteriae
|
|
Clostridium histolyticum
|
Escherichia coli type 0124:NM (ETEC)
|
Shigella flexneri
|
|
Clostridium novyi
|
Escherichia coli type 078:k80:h12 (EIEC)
|
Yersinia enterocolitica
|
Beschränkung des Tests
Wie in jedem Falle einer Diagnose, sollte der Arzt die mit diesem Test erhaltenen Befunde mit anderen klinischen Methoden bestätigen. Ein negatives Ergebnis schließt keine Infektion aus. Falls die begründete Annahme einer Infektion besteht, sollte eine weitere Stuhlprobe untersucht werden.
Ein positives Ergebnis schließt das Vorhandensein von anderen Krankheitserregern nicht aus.
Literatur
- Gerding, et al. „Clostridium difficile-Associated Diarrhea and Colitis“. Infection Control and Hospital Epidemiology 1995:16, 459-477.
- Barbut, et. al. „Prevalence and Genetic Characterization of Toxin A Variant Strains of Clostridium difficile among Adults and Children with Diarrhea in France“. J Clin Microbiol2002:40, 2079-83.
- Bartlett, JG., Gerding, DN. „Clinical Recognition and Diagnosis of Clostridium difficile Infection“. CID 2008:46 (Suppl 1), S12-S18
Qualitätssicherung und Vorkommnisse
Sollten Sie den Eindruck eines Qualitätsmangels haben oder unklare oder ihrerseits falsch-positive oder falsch-negative Ergebnisse erhalten, bitten wir Sie, die betreffende Patientenprobe zurückzustellen und für einen Abruf für uns bereitzuhalten.
Bitte informieren Sie uns umgehend. Sie helfen uns dadurch die Sicherheit der Produkte und damit die Qualität zu gewährleisten.
 |
Hersteller: |

Günter Keul GmbH
Von-Langen-Weg 10
D-48565 Steinfurt
Tel.: 02551/2097 Fax.: 02551/80883
Web: www.keul.de
|
(akt. 05.09.2014)
|
|