| |
Keul-o-test
hCG-Testkassette
KGST104
DIMDI-Reg.-Nr. DE/CA22/1115-294-IVD
Ein Schnelltest für den qualitativen Nachweis von humanem Chorion-Gonadotropin (hCG) im Urin.
Nur für den professionellen in-vitro-diagnostischen Gebrauch.
VERWENDUNGSZWECK
Die hCG-Schwangerschafts-Schnelltestkassette ist ein schneller chromatographischer Immunoassay für den qualitativen Nachweis von humanem Chorion-Gandotropin im Urin als Hilfe zur frühen Erkennen einer Schwangerschaft.
ZUSAMMENFASSUNG
Humanes Chorionic Gonadotropin (hCG) ist ein Glycoprotein-Hormon, das von der sich entwickelnden Plazenta kurz nach der Befruchtung produziert wird. Bei einer normalen Schwangerschaft kann hCG sowohl im Urin als auch im Serum oder Plasma ab dem 7 bis 10 Tag nach der Empfängnis nachgewiesen werden. 1,2,3,4 Die hCG Gehalte steigen sehr stark an, überschreiten häufig 100mIU/ml beim ersten Ausbleiben der Menstruation,2,3,4 und erreichen in etwa der 10 – 12 Schwangerschaftswoche mit 100,000-200,000mIU/ml ihren Höhepunkt. Das Auftreten von hCG nach der Empfängnis sowohl im Urin als auch im Serum oder Plasma und das nachfolgende schnelle Ansteigen der Konzentration während der ersten Schwangerschaftswochen, stellt einen hervorragenden Hinweis beim frühen Erkennen einer Schwangerschaft dar.
Die hCG Schwangerschafts-Schnelltestkassette ist ein Schnelltest, der das qualitative Vorhandensein von hCG in Urinproben mit einer Sensitivität von 10mIU/ml nachweist. Der Test nutzt eine Kombination von monoklonalen und polyklonalen Antikörpern, um selektiv erhöhte Gehalte von hCG im Urin nachzuweisen. Bei dem angegebenen Sensitivitätswert zeigt die hCG-Schwangerschafts-Schnelltestkassette keine Beeinträchtigung durch Kreuzreaktivität durch strukturell verwandte hFSH, hLH und hTSH in hohen physiologischen Konzentrationen.
ARBEITSWEISE
Die hCG Schwangerschafts-Schnelltestkassette ist ein schneller chromatographischer Immunoassay für den qualitativen Nachweis von humanem Chorionic Gonadotropin im Urin als eine Hilfe bei einer frühen Bestimmung einer Schwangerschaft. Der Test nutzt zwei Linien um die Ergebnisse anzuzeigen. Der Test verwendet eine Kombination von Antikörpern einschließlich einem monoklonalen hCG Antikörper, um selektiv erhöhte hCG-Gehalte nachzuweisen. Die Kontrolllinie besteht aus ziegenpolyklonalen Antikörpern und kolloidalen Goldpartikeln. Der Test wird durch Zugabe der Urinprobe durchgeführt und führt zur Ausbildung von farbigen Linien. Die Probe wandert mittels Kapillarwirkung durch die Membran, um mit dem Konjugat zu reagieren und eine Farbbande auszubilden. Positive Proben reagieren mit dem spezifischen Antikörper-hCG-Konjugat und bilden eine farbige Linie im Testlinienbereich auf der Membran. Das Fehlen dieser Line zeigt ein negatives Ergebnis an. Um eine Verfahrenskontrolle zu bieten, erscheint immer im Kontrolllinienbereich eine farbige Linie, die anzeigt, dass eine ausreichende Probenmenge hinzugefügt wurde und eine Membrandurchfeuchtung erfolgte.
REAGENZIEN
Der Test enthält eine mit anti-hCG Partikel und anti-hCG beschichtete Membran.
VORSICHTSMASSNAHMEN
Bitte lesen Sie alle Informationen in dieser Packungsbeilage bevor Sie den Test durchführen.
- Nur für den professionellen in-vitro-diagnostischen Gebrauch. Nicht nach Ablauf des Verwendbarkeitsdatums benutzen.
- Der Test sollte im versiegelten Folienbeutel bleiben, bis er benutzt wird.
- Alle Proben sollten als potentiell gefährlich betrachtet werden und in derselben Weise wie infektiöses Material behandelt werden.
- Der benutzte Test sollte entsprechend den örtlichen Vorschriften entsorgt werden.
LAGERUNG UND STABILITÄT
Lagern Sie den Test wie abgepackt bei Raumtemperatur oder gekühlt (2-30°C). Der Test ist bis zu dem auf der versiegelten Folientasche oder dem Etikett auf der geschlossenen Verpackung angegebenen Haltbarkeitsdatum stabil. Der Test muss bis zur Verwendung im versiegelten Folienbeutel oder in der verschlossenen Verpackung verbleiben. NICHT EINFRIEREN. Nicht nach Ablauf des Haltbarkeitsdatums verwenden.
PROBENAHME UND VORBEREITUNG
Urinproben
Die Urinprobe muss in einem sauberen und trockenen Behälter gesammelt werden. Der erste Morgenurin wird bevorzugt, weil er generell die höchste hCG-Konzentration enthält. Trotzdem können auch zu anderen Tageszeiten genommene Urinproben verwendet werden. Urinproben die sichtbare Bestandteile enthalten sollten zentrifugiert, gefiltert oder stehengelassen werden, so dass sich der Niederschlag absetzt, um so für das Testen eine klare Probe zu erhalten.
Probenlagerung
Urinproben können bei 2-8°C bis zu 48 Stunden vor dem Testen gelagert werden. Für eine längere Lagerung können die Proben eingefroren und unter -20°C gelagert werden. Eingefrorene Proben sollten vor dem Testen aufgetaut und gemischt werden.
MATERIALIEN
Vorhandene Materialien
- Testkassetten
- Pipetten
- Gebrauchsanweisung
Erforderliche, aber nicht vorhandene Materialien
- Probensammelbehälter
- Timer
GEBRAUCHSANWEISUNG
- Bringen Sie den Folienbeutel vor dem Öffnen auf Raumtemperatur (15-30°C). Entnehmen Sie die Kassette aus dem versiegelten Folienbeutel und verwenden Sie sie innerhalb einer Stunde.
- Legen Sie die Kassette auf eine saubere und ebene Oberfläche. Halten Sie die Pipette senkrecht und geben Sie langsam 3 volle, hängende Tropfen Urin (etwa 120ul) in die Probenvertiefung der Kassette und starten Sie dann den Kurzzeitwecker. Warten Sie bei der Zugabe des jeweils nächsten Tropfens, bis der vorige vollständig aufgenommen wurde. Vermeiden Sie die Bildung von Luftblasen in der Probenvertiefung. Beachten Sie die Abbildung unten.
- Lesen Sie das Ergebnis nach 3 Minuten ab. Lesen Sie das Ergebnis nicht nach mehr als 10 Minuten ab.
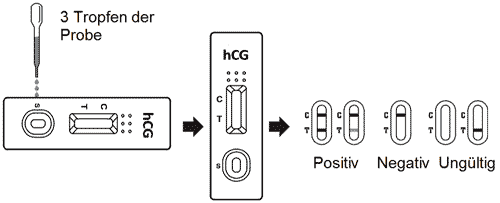 ABLESEN DER ERGEBNISSE
(Bitte beachten Sie die Abbildung oben)
POSITIV: Es erscheinen deutliche farbige Linien. Eine Linie sollte im Kontrolllinienbereich (C) und eine weitere Linie sollte im Testlinienbereich (T) sein. Eine Linie kann heller als die andere sein; sie müssen nicht übereinstimmen. Dies bedeutet, dass Sie wahrscheinlich schwanger sind.
NEGATIV: Eine farbige Linie erscheint im Kontrolllinienbereich (C). Keine Linie erscheint im Testlinienbereich (T). Dies bedeutet, dass Sie wahrscheinlich nicht schwanger sind.
UNGÜLTIG: Wenn keine farbige Linie im Kontrolllinienbereich (C) erscheint, ist der Test ungültig, sogar wenn eine Linie im Testlinienbereich (T) auftritt. Sie sollten den Test mit einer neuen Testkassette wiederholen.
QUALITÄTSKONTROLLE
Der Test beinhaltet eine interne Verfahrenskontrolle. Wenn eine farbige Linie im Kontrollbereich (C) erscheint, ist diese als eine interne Verfahrenskontrolle zu betrachten. Sie bestätigt eine genügende Probenmenge und einen korrekten Verfahrensablauf. Ein Ausbleiben der Kontrolllinie ist ein Nachweis für eine falsche Verfahrensdurchführung. Wenn die Farbbande im Ergebnisfenster erscheint und keine Kontrolllinie, kann das Ergebnis ungültig sein.
Laut RiliBÄK sollte jede neue Charge mittels einer positiven hCG Kontrolle (mit 10-250 mIU/ml hCG) und einer negativen hCG Kontrolle (mit „0“mIU/ml hCG) getestet werden, um damit die ordnungsgemäße Leistungsfähigkeit des Tests zu zeigen.
BESCHRÄNKUNGEN
- Die hCG Schwangerschafts-Schnelltestkassette ist ein erster qualitativer Test. Dieser Test kann weder einen quantitativen Wert noch einen Anstieg des hCG bestimmen.
- Sehr stark verdünnte Urinproben, die durch ein geringes spezifisches Gewicht zu erkennen sind, können keinen erkennbaren Gehalt von hCG enthalten. Falls eine Schwangerschaft weiterhin angenommen wird, sollte 48 Stunden später eine erste Morgenurinprobe gewonnen und getestet werden
- Sehr niedrige hCG-Gehalte (weniger als 50mIU/ml) sind kurz nach einer Implantation in Urinproben vorhanden. Da jedoch eine beträchtliche Anzahl von Schwangerschaften im ersten Trimenon aus natürlichen Gründen enden,5 sollte ein schwach positives Ergebnis durch ein erneutes Testen mit einer 48 Stunden später gesammelten ersten Morgenurinprobe wiederholt werden.
- Dieser Test kann zu falsch-positiven Ergebnissen führen, wenn eine Reihe von Bedingungen erfüllt sind. So können zum Beispiel Trophoblasterkrankungen und bestimmte nicht trophoblastische Neoplasmen einschließlich Hodentumoren, Prostatakrebs, Brustkrebs und Lungenkrebs erhöhte hCG-Gehalte bewirken.6,7 Das Vorhandensein von hCG im Urin sollte daher nicht für die Diagnose einer Schwangerschaft verwendet werden, solange diese Bedingungen nicht ausgeschlossen werden können.
- Falsch-negative Ergebnisse können vorkommen, wenn die hCG-Gehalte unter der Sensitivitätsgrenze des Tests liegen. Wenn eine Schwangerschaft weiterhin angenommen wird sollte eine erste Morgenurinprobe 48 Stunden später gesammelt und getestet werden.
- Dieser Test bietet eine wahrscheinliche Diagnose für eine Schwangerschaft. Eine bestätigte Schwangerschaftsdiagnose sollte nur nach Auswertung aller klinischen und Laborbefunde erfolgen.
ERWARTETE WERTE
Negative Ergebnisse werden bei gesunden nicht schwangeren Frauen und gesunden Männern erwartet. Gesunde schwangere Frauen haben hCG in ihren Urin- und Serumproben. Der Gehalt von hCG schwankt stark mit dem Schwangerschaftsalter und zwischen Personen. Die hCG-Schwangerschafts-Schnelltestkassette für Urin hat eine Sensitivität von 10mIU/ml, und ist geeignet eine Schwangerschaft bereits am ersten Tag nach dem Ausbleiben der Menstruation zu erkennen.
LEISTUNGSCHARAKTERISTIKA
Genauigkeit
Es wurde eine multizentrische klinische Evaluation durchgeführt, bei der die mit der hCG-Schwangerschafts-Schnelltestkassette erlangten Ergebnisse mit denen eines anderen kommerziell verfügbaren Urin-hCG Schnelltests verglichen wurden. Die Urinstudie umfasste 608 Proben und beide Tests erkannten 377 negative und 231 positive Ergebnisse. Die Ergebnisse zeigten eine Gesamtgenauigkeit von >99% der hCG-Schwangerschafts-Schnelltestkassette im Vergleich mit dem anderen hCG Schnelltest.
hCG Referenzmethode (Urin)
| Methode |
anderer hCG Schnelltest |
Gesamtergebnisse |
| hCG Schwangerschafts-Schnelltestkassette |
Ergebnisse |
Positiv |
Negativ |
| Positiv |
231 |
0 |
231 |
| Negativ |
0 |
377 |
377 |
| Gesamtergebnisse |
231 |
377 |
608 |
Sensitivität: >99.9% (98.7%~100%)* Spezifität: >99.9%(99.2%~100%)*
Genauigkeit: >99.9 %( 99.5%~100%) * * 95% Konfidenzintervalle
Sensitivität und Kreuzreaktivität
Die hCG-Schwangerschafts-Schnelltestkassette weist hCG mit einer Konzentration von 10mIU/ml oder mehr nach.
Der Test wurde nach dem W.H.O. International Standard standardisiert. Die Zugabe von LH (300mIU/ml), FSH (1,000mIU/ml), und TSH (1,000μIU/ml) zu negativen (0mIU/ml hCG) und positiven (10mIU/ml hCG) Proben zeigte keine Kreuzreaktivität.
Präzision / Intra-Assay
Die chargeninterne Präzision wurde durch die Verwendung von 10 Wiederholungen von drei Proben bestimmt, die 10mIU/ml, 100mIU/ml, 250mIU/ml und 0mIU/ml HCG enthielten. Die negativen und positiven Werte wurden insgesamt zu 100% korrekt erkannt.
Präzision / Inter-Assay
Die Präzision zwischen den Chargen wurde unter Verwendung derselben drei Proben mit 10mIU/ml, 100mIU/ml, 250mIU/ml und 0mIU/ml HCG mit 10 verschiedenen Tests bestimmt. Drei unterschiedliche Chargen der hCG-Schwangerschafts-Schnelltestkassette wurden getestet. getestet. Die Proben wurden insgesamt zu 100% korrekt erkannt.
Störende Substanzen
Die folgenden potentiell störenden Substanzen wurden zu hCG negativen und positiven Proben zugesetzt.
Acetaminophen 20 mg/dl
Acetylsalicylsäure 20 mg/dl
Askorbinsäure 20 mg/dl
Atropin 20 mg/dl
Bilirubin 2 mg/dl
Coffein 20 mg/dl
Gentisinsäure 20 mg/dl
Glukose 2 g/dl
Hämoglobin 1 mg/dl
Bilirubin (Serum oder Plasma ) 40mg/dl
Keine der Substanzen beeinträchtigte in der untersuchten Konzentration den Test.
LITERATUR
- Batzer FR. Hormonal evaluation of early pregnancy, Fertil. Steril. 1980; 34(1): 1-13
- Catt KJ, ML Dufau, JL Vaitukaitis Appearance of hCG in pregnancy plasma following the initiation of implantation of the blastocyte, J. Clin. Endocrinol. Metab. 1975; 40(3): 537-540
- Braunstein GD, J Rasor, H. Danzer, D Adler, ME Wade Serum or plasma human chorionic gonadotropin levels throughout normal pregnancy, Am. J. Obstet. Gynecol. 1976; 126(6): 678-681
- Lenton EA, LM Neal, R Sulaiman Plasma concentration of human chorionic gonadotropin from the time of implantation until the second week of pregnancy, Fertil. Steril. 1982; 37(6): 773-778
- Steier JA, P Bergsjo, OL Myking Human chorionic gonadotropin in maternal plasma after induced abortion, spontaneous abortion and removed ectopic pregnancy,Obstet.Gynecol.1984; 64(3): 391-394
- Dawood MY, BB Saxena, R Landesman Human chorionic gonadotropin and its subunits in hydatidiform mole and choriocarcinoma, Obstet. Gynecol. 1977; 50(2): 172-181
- Braunstein GD, JL Vaitukaitis, PP Carbone, GT Ross Ectopic production
QUALITÄTSSICHERUNG UND VORKOMMNISSE
Sollten Sie den Eindruck eines Qualitätsmangels haben oder unklare oder ihrerseits falsch-positive oder falsch-negative Ergebnisse erhalten, bitten wir Sie, die betreffende Patientenprobe zurückzustellen und für einen Abruf für uns bereitzuhalten.
Bitte informieren Sie uns umgehend. Sie helfen uns dadurch die Sicherheit der Produkte und damit die Qualität zu gewährleisten.
SYMBOLERKLÄRUNG
 |
Hersteller: |

Günter Keul GmbH
Von-Langen-Weg 10
D-48565 Steinfurt
Tel.: 02551/2097 Fax.: 02551/80883
Web: www.keul.de |
(akt. 27.04.2016)
|
|